サステナビリティ
コーポレート・ガバナンス
ガバナンス体制
久光製薬では、コーポレート・ガバナンスを強化するとともに、経営の透明性向上とコンプライアンスの徹底およびリスクマネジメントの推進などを通じて企業価値向上に取り組み、善き企業市民としてステークホルダーの皆さまとの信頼関係の構築に努めてまいります。
コーポレート・ガバナンス体制
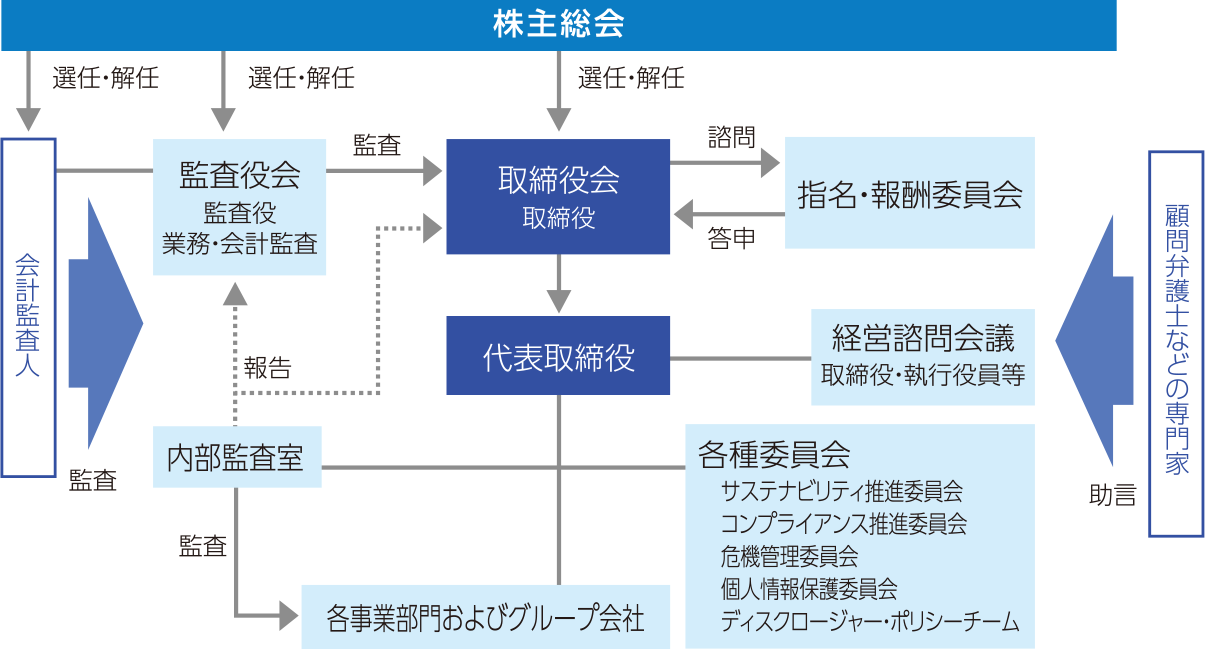
久光製薬は、透明・公正かつ迅速・果断な意思決定を行うための仕組みとして、コーポレート・ガバナンス体制の充実に努めています。当社は監査役会設置会社の形態をとっており、取締役10名(うち、社外取締役4名)と監査役4名(うち、社外監査役2名)がそれぞれ取締役会、監査役会を構成しています。取締役会はそれぞれの能力や経験、見識の多様性を考慮して構成されており、取締役の経営責任をより明確にし、経営環境の変化に対応できる経営体制を構築するために、任期を1年としています。経営における意思決定は、必要に応じ主要な取締役・執行役員等から構成される経営諮問会議での討議を踏まえて行われ、特に重要な事項は取締役会において審議、決定します。さらに、経営判断の迅速化、透明性、戦略性の向上を目的とした執行役員制度を導入しています。また、取締役会の諮問機関として、委員の過半数を独立社外取締役で構成する「指名・報酬委員会」を設置し、経営の透明性・客観性の向上に努めています。当社の監査役制度は、監査役がより公正な監査を実施する目的で、取締役会に出席するほか、定期的な監査役会の開催、内部監査室や会計監査人と連携した監査の実施など、グループ全体の監査体制の強化を図っています。
コーポレート・ガバナンス体制図
役員一覧 ・・・ 2025年6月25日現在
取締役
| 代表取締役社長 | 中冨 一榮 |
|---|---|
| 常務取締役執行役員 国内営業管掌 | 齋藤 久 |
| 取締役執行役員 法務担当 兼 生産環境・信頼性保証管掌 兼 コンプライアンス担当 |
堤 信夫 |
| 取締役執行役員 内部統制担当 兼 国内子会社担当 | 村山 進一 |
| 取締役執行役員 社長室 室長 兼 人事担当 兼 研究開発担当 兼 DX担当 兼 サステナビリティ推進管掌 |
瀧山 浩二 |
| 取締役執行役員 経営企画本部 本部長 | 磯部 雄一 |
| 社外取締役 (非常勤) |
安西 祐一郎 |
| 社外取締役 (非常勤) |
松尾 哲吾 |
| 社外取締役 (非常勤) |
渡邊 珠子 |
| 社外取締役 (非常勤) |
野口 みどり |
監査役
| 監査役 | 中冨 舒行 |
|---|---|
| 監査役 | 平野 宗彦 |
| 社外監査役 (非常勤) |
渡邉 健太郎 |
| 社外監査役 (非常勤) |
板倉 龍介 |
執行役員
| 専務執行役員 業務本部管掌 | 秋山 哲雄 |
|---|---|
| 常務執行役員 グローバルテクノロジー統括長 兼 MN事業化推進室 室長 | 肥後 成人 |
| 上席執行役員 バレーボール事業担当 | 萱嶋 章 |
| 上席執行役員 薬粧事業部 事業部長 | 奥野 昌哉 |
| 上席執行役員 医薬事業部 事業部長 | 鶴田 光利 |
| 上席執行役員 BU本部 本部長 | 矢野 栄 |
| 上席執行役員 国際事業部 事業部長 | 平松 太郎 |
| 執行役員 研究開発本部 本部長 | 寺原 孝明 |
| 執行役員 渉外担当 | 南 秀尚 |
| 執行役員 生産環境本部 本部長 | 尾﨑 太郎 |
| 執行役員 国際事業部 APEA営業統括部 部長 兼 シンガポール支店 支店長 兼 マニラ支店 支店長 |
佐藤 勝宏 |
| 執行役員 関連事業担当 | 舛屋 泰之 |
| 執行役員 国際事業部 国際業務改革部 部長 | 森脇 康次 |
| 執行役員 ノーベン ファーマシューティカルス担当 | 増本 武 |
| 執行役員 ノーベン ファーマシューティカルス ビジネスデベロップメント担当 |
樫山 誠司 |
| 執行役員 薬粧事業部 広域量販部 部長 | 鈴木 智也 |
| 執行役員 医薬事業部 広域流通推進部 部長 | 松尾 良介 |
| 執行役員 サステナビリティ推進担当 兼 BU本部 九州本社総務部 部長 | 森崎 亜紀子 |
| 執行役員 信頼性保証本部 本部長 | 中原 敏博 |
| 執行役員 BU本部 財務部 部長 | 根本 剛 |
| 執行役員 DX推進部 部長 | 井町 信彦 |
経営諮問会議
経営における意思決定は、必要に応じ主要な取締役・執行役員等から構成される経営諮問会議での討議を踏まえて行われ、特に重要な事項は取締役会において審議、決定されています。
スキルマトリックス
| 氏名 | 企業経営 | 販売・ マーケティング |
グローバル・ ビジネス |
生産・ 研究開発 |
IT・DX | 人事・ 人材育成 |
サステナ ビリティ ・ESG |
法律・ コンプライアンス・ リスクマネジメント |
財務・ 会計 |
|
|---|---|---|---|---|---|---|---|---|---|---|
| 取締役 | 中冨 一榮 | ● | ● | ● | ● | |||||
| 齋藤 久 | ● | ● | ● | |||||||
| 堤 信夫 | ● | ● | ● | |||||||
| 村山 進一 | ● | ● | ● | |||||||
| 瀧山 浩二 | ● | ● | ● | ● | ||||||
| 磯部 雄一 | ● | ● | ● | |||||||
| 安西 祐一郎 | ● | ● | ● | ● | ||||||
| 松尾 哲吾 | ● | ● | ||||||||
| 渡邊 珠子 | ● | ● | ● | |||||||
| 野口 みどり | ● | ● | ● | ● | ||||||
| 監査役 | 中冨 舒行 | ● | ||||||||
| 平野 宗彦 | ● | |||||||||
| 渡邉 健太郎 | ● | ● | ||||||||
| 板倉 龍介 | ● | ● | ● |
取締役の個人別の
報酬等の内容に係る決定方針
久光製薬は、2021年2月18日開催の取締役会にて、取締役の個人別の報酬等の内容に係る決定方針を以下のとおり定めております。当社の取締役の報酬は、企業価値の持続的な向上を図るインセンティブとして十分に機能するよう株主利益と連動した報酬体系とし、個々の取締役の報酬の決定に際しては各職責を踏まえた適正な水準とすることを基本方針としております。具体的には、業務執行取締役の報酬は、固定報酬としての基本報酬、業績連動報酬および株式報酬により構成し、監督機能を担う社外取締役については、その職務に鑑み、基本報酬のみを支払うこととしております。 業務執行取締役の種類別の報酬割合については、当社と同程度の事業規模および従業員規模、関連する業種に属する企業等を参考とした報酬水準を踏まえ、指名・報酬委員会において検討を行うこととしております。 なお、報酬等の種類ごとの比率の目安は、基本報酬:業績連動報酬等:非金銭報酬等=50%:30%:20%(業績指標を100%達成の場合)としております。
2024年度取締役及び監査役の報酬等の総額等
| 区分 | 報酬等の総額 (百万円) |
報酬等の種類別の総額(百万円) | 対象となる 役員の員数 (人) |
||
|---|---|---|---|---|---|
| 基本報酬 | 業績連動報酬等 | 非金銭報酬等 | |||
| 取締役 (うち社外取締役) |
258 (19) |
131 (19) |
54 (-) |
73 (-) |
9 (3) |
| 監査役 (うち社外監査役) |
60 (14) |
60 (14) |
- (-) |
- (-) |
5 (3) |
| 合計 (うち社外役員) |
319 (34) |
192 (34) |
54 (-) |
73 (-) |
14 (6) |
- (注)1.当事業年度末日時点における在籍人員は、取締役9名、監査役4名であります。
- 2.業績連動報酬等は、事業年度ごとの業績向上に対する意識を高めるための業績指標を反映した現金報酬とし、事業年度毎の業績目標達成度等に応じて算出された額を賞与として毎年、一定の時期に支給しております。
目標となる業績指標とその値は、中期経営計画と整合するよう計画策定時に設定し、適宜、環境の変化に応じて指名・報酬委員会の答申を踏まえた見直しを行うものとしております。 - 3.非金銭報酬等は、株価変動のメリットとリスクを株主の皆さまと共有し、株価上昇および企業価値向上への貢献意欲を従来以上に高めることを目的に、株式報酬型ストックオプションとしての新株予約権を割り当てるものとしております。当該ストックオプションの内容およびその交付状況は、電子提供措置事項「会社の新株予約権等に関する事項」に記載のとおりです。
取締役会の実効性評価
久光製薬は取締役会全体が適切に機能しているかを定期的に検証し、その結果を踏まえ、問題点の改善や強みの強化等の適切な措置を講じていくという継続的プロセスにより、取締役会全体の機能向上を図っています。
実効性評価の目的および方法
取締役会の実効性向上のために、取締役会の構成、運営状況等の実質的な評価を行うことを目的として、毎年、取締役会事務局がアンケートを実施し、結果を取締役会で報告・討議しています。
検討項目
- ● 取締役会の構成と運営
- ● 経営戦略と事業戦略
- ● 企業倫理とリスク管理
- ● 業績モニタリングと経営陣の報酬
- ● 株主等との対話
- ● ステークホルダーとの適切な協働
- ● 適切な情報開示と透明性の確保
評価結果
アンケート結果について取締役会において討議を行った結果、取締役会の実効性は十分に確保されていると評価しています。アンケート結果に基づき、さらなる改善に向けて以下の討議を行いました。
- ● 中期経営方針、事業開発の進捗に関する議論の一層の充実
- ● 女性管理職比率も含めた人事政策の強化
- ● リスクマネジメントの強化
これらを踏まえ、当社中期経営方針進捗、事業開発進捗、人事政策、サステナビリティ、リスクマネジメント等についての議論をより充実させ、当社取締役会のさらなる機能・実効性の確保・向上に努めてまいります。
内部統制システム
久光製薬は、取締役会で決議された内部統制規定書(内部統制基本方針)に基づき、コーポレート・ガバナンスの充実を図りながら、経営環境の変化に迅速に対応できる組織体制の構築に取り組んでいます。当社およびグループ各社における、企業活動に際しての法の遵守、企業倫理の浸透、コンプライアンスの遵守の徹底および経営の透明性の向上に努めています。
内部統制規定書
久光製薬株式会社は、会社法及び会社法施行規則に基づき、以下のとおり、当社の業務の適正を確保するための体制を整備する。
- 1. 取締役の職務の執行に係る情報の保存及び管理に関する体制
- 2. 損失の危険の管理に関する規程その他の体制
- 3. 取締役の職務の執行が効率的に行われることを確保するための体制
- 4. 取締役及び使用人の職務の執行が法令及び定款に適合することを確保するための体制
- 5. 当該株式会社並びにその親会社及び子会社から成る企業集団における業務の適正を確保するための体制
- 6. 監査役がその職務を補助すべき使用人を置くことを求めた場合における当該使用人に関する事項
- 7. 前記6の使用人の取締役からの独立性に関する事項
- 8. 監査役の前記6の使用人に対する指示の実効性の確保に関する事項
- 9. 監査役への報告に関する体制
- 10. 前記9の報告をした者が当該報告をしたことを理由として不利な取扱いを受けないことを確保するための体制
- 11. 監査役の職務の執行について生ずる費用の前払又は償還の手続その他の当該職務の執行について生ずる費用又は債務の処理に係る方針に関する事項
- 12. その他監査役の監査が実効的に行われることを確保するための体制
内部監査
内部監査部門として専任担当者を配置した内部監査室を設置し、業務活動の有効性や適正性、コンプライアンス等の適合性の観点から、当社およびグループ各社の業務執行状況の監査を実施しています。また、監査役会と内部監査室が協力しリスクの高い事業、業務プロセスを選定し深度の深いテーマ監査の実施、経営リスクマネジメント、従業員の年次有給休暇の取得状況およびストレスチェックに関しても監査を実施しています。その結果は取締役会・監査役会への報告を行うとともに担当部門長および担当取締役に報告し、必要に応じて内部統制の改善指導および実施の支援・助言を行っています。さらに、グループ各社の監査も定期的に行い、意思決定、経理等の重要手続きに対する支援・助言を通じて、健全な業務環境を維持するよう努めています。
会計監査
会計監査を担当する会計監査人として、有限責任 あずさ監査法人と監査契約を結んでおり、正しい経営情報を提供するなど公正な立場から監査が実施される環境を提供しています。監査業務を執行した会計監査人は、指定社員・業務執行社員2名、公認会計士8名、その他19名であり、会計監査人の継続監査年数はすべて7年以内です。なお、有限責任あずさ監査法人および指定有限責任社員・業務執行社員と当社の間には特別な利害関係はありません。