企業情報
コーポレート・ガバナンス
コンプライアンス
久光製薬は、人々の健康にかかわる医薬品企業として、生命の尊厳を尊重し、科学に対する謙虚さと社会に対する良識を持って事業に従事することが求められます。さまざまな事業活動において、関連する各国の法規制はもとより社会の基本的ルールや規則を誠実に遵守するとともに、高い倫理観を持って行動し、「世界の人々のQOL向上を目指す」という経営理念の実現に努めています。
コンプライアンスの推進
コンプライアンスの徹底と倫理性を確保するため、企業としての基本姿勢を定めた「久光企業憲章」および遵守すべき行動規準として「コンプライアンス・プログラム」を制定しました。推進にあたり、コンプライアンス推進委員会および事務局としてコンプライアンス推進室を設置し、コンプライアンス推進担当の取締役を委員長として任命しています。
「コンプライアンス・プログラム」では法令を遵守し、高い倫理観を持って行動するとともに、贈収賄や利益供与、利益相反行為などあらゆる不正・腐敗行為の禁止を明言しています。コンプライアンスの実践に際しては、「久光企業憲章」および「コンプライアンス・プログラム」をハンドブックとして全役員・従業員に配布して各職場で読みあわせを実施しているほか、全管理者への教育研修を毎年継続して行っています。また、内部監査室が客観的な立場から実践状況を調査しています。
さらに、社内通報窓口「久光ほっとライン」を設置し、従業員の声をコンプライアンスの実践に反映させる体制を整備しています。
久光企業憲章
当社は、世界中の人々のQOL向上に貢献し続ける為に、以下の条項に基づき、国内外を問わず、人権を尊重するとともに、すべての法令・規準を遵守するものとし、高い倫理観をもって行動します。
1 医薬品企業としての企業行動
- ① 人々の健康に貢献する医薬品の研究開発に積極的に取り組み、有効性・安全性にすぐれた、高品質の医薬品の安定供給を行います。また、医療経済効果の高い医薬品の開発を通じ、医療コストの効率向上に寄与します。
- ② 臨床試験は医療機関の協力のもと、被験者の人権を尊重し、安全確保に留意し、かつ科学的厳正さをもって遂行します。また、非臨床試験として必要な動物実験は動物福祉に十分配慮して行います。
- ③ 医薬品の適正使用の確保に向けて、品質・有効性・安全性に関する科学に裏付けされた国内外の的確な情報を提供するとともに、製造販売後の情報の収集、分析評価、伝達を迅速に行います。
- ④ 医薬品企業にふさわしい公正、透明で自由な競争を行うとともに、従業員の倫理観の向上に努め、政治・行政・医療関係者等との健全かつ正常な関係を保ちます。
2 企業市民としての企業行動
- ⑤ 高度IT化に伴い、個人情報や顧客情報の適正な保護に十分配慮し、万全の対策を行います。
- ⑥ 会社の内部情報を適切に管理し、当社を取り巻くステークホルダーとのコミュニケーションを広く行い、広報活動等により適時・適切に企業情報を開示します。
- ⑦ 特許や著作権などを含む知的財産権を尊重し、価値を認めます。また、これを不正に入手し、利用しません。
- ⑧ 従業員の多様性・人格・個性を尊重するとともに、従業員のゆとりと豊かさを実現し、安全で働きやすい環境を確保します。また、従業員の倫理観の高揚と資質の向上に努めます。
- ⑨ 総会屋や暴力団等の市民社会の秩序や安全に脅威を与える反社会的勢力および団体とは断固として対決します。
- ⑩ 環境問題への取り組みは人類共通の課題であることを認識して、資源やエネルギーの効率的利用を行い、自主的、積極的に環境保全に取り組みます。
- ⑪ 国内・海外を問わず、現地の法律や行動規範の遵守はもとより、現地の文化や慣習を尊重し、現地の発展に貢献する経営を行います。
- ⑫ 良き企業市民として、社会に貢献する活動に積極的に取り組みます。
3 経営トップとしての行動
- ⑬ 経営トップは、本憲章の精神の実現を率先垂範し、関係者へ周知徹底します。また、社内外の声を把握し、実効ある社内体制の整備を行うとともに、企業倫理の徹底を図ります。
- ⑭ 本憲章の精神に反する事態が起きた時は、経営トップ自らの責任において問題解決に当たり、原因究明・再発防止に努めます。
- ⑮ 本憲章の精神に反する事態が起きた時は、社会への迅速かつ的確な情報開示と説明を行います。
また、通報者のプライバシー事項に関しては必要な関係者以外には開示せず、相談・提言等を理由に通報者が不利益になる取り扱いは行いません。
今後も、当社およびグループ各社における企業倫理、環境保全、個人情報保護など社会的責任にかかわるコンプライアンスの更なる充実・維持強化を図っていきます。
透明性のある事業活動
日本製薬工業協会が2013年に策定した「製薬協コード・オブ・プラクティス」の趣旨に従い、法令遵守はもとより、より高い倫理観を持って行動するため「久光製薬コード・オブ・プラクティス」(久光コード)を制定しました。これは、プロモーション活動のみならず、当社と研究者、医療関係者、医療機関、患者団体、卸売業者等との交流において遵守すべき自主規範で、高い倫理性と透明性をもって企業活動を遂行することを求めています。
さらに、医療用医薬品のプロモーションを実施する際に遵守すべき自主基準として「医療用医薬品プロモーションコード」を定め、すべての役員・従業員がこの基準を遵守し、適切なプロモーションを行うこととしています。国外における活動でも、久光コードを尊重するとともに、当該国の関係法規に加え、当該国に製薬団体のコードがある場合にはそのコードを、かかるコードがない場合にはIFPMA(国際製薬団体連合会)のコード・オブ・プラクティスを遵守しています。
また、当社と医療機関等や患者団体との関係においては、高い倫理観を持って透明性のある関係を構築しています。当社の活動がライフサイエンスの発展に寄与し、高い倫理性を担保しているうえで行われていることを広く理解していただくため、日本製薬工業協会が策定したガイドラインに基づき「企業活動と医療機関等の関係の透明性に関する指針」および「企業活動と患者団体の関係の透明性に関する指針」を定め、当社が行った資金提供等については、当社WEBサイトを通じて毎年公開しています。
【参考】
企業活動と医療機関等の関係
https://www.hisamitsu.co.jp/company/guideline-e.html
企業活動と患者団体との関係
https://www.hisamitsu.co.jp/company/guideline-p.html
知的財産の保護
当社では、知的財産権を経営戦略の一つの大きな柱として位置づけ、商品開発、製造技術、品質管理およびマーケティング活動に至る成果を当社のブランドとして保護し育てるため、特許・意匠・商標などの知的財産を権利として得ることにより、創薬・育薬された当社医薬品等の安定した供給を実現しています。
具体的には、商品の開発・改良の早期段階から研究開発部門と知的財産部門が積極的に協力し、発明・創作から生まれた成果を戦略的に特許出願することにより、市場における事業の優位性を確保し、さらには、商品のブランドの保護強化のため、意匠や商標を登録出願し、これら知的財産を多面的に権利化するよう努めています。
また、企業や商品の情報を的確に伝達するためには、音や動きなどの「新しいタイプの商標」の価値や重要性にもいち早く着目し、日本を含む世界各国でこれらを積極的に登録出願するなどの先進的な取り組みも行っています。
このように、当社では、知的財産の権利化を推進することで当社ブランドの信用の維持向上に努めています。


動物福祉への倫理的配慮
久光製薬では、動物福祉の精神を徹底し、動物福祉へ配慮した適正な動物実験が実施されるよう「動物の愛護及び管理に関する法律」に準拠した「動物実験指針」を制定しています。
薬の有効性や安全性を確認する動物実験を行う場合、全ての実験を「動物実験委員会」で審査することを制度化しており、3Rの理念(Replacement:代替法の選択、Reduction:動物数の削減、Refinement:苦痛の軽減)のもと研究を進めています。動物実験の実施体制については、定期的な自己点検に加えて、第三者機関であるヒューマンサイエンス振興財団(動物実験実施施設認証センター)による審査を受け、動物実験実施施設認定を取得しています。今後もさらなる動物実験の適正化と動物福祉の維持・向上に努めていきます。
倫理的・科学的な臨床試験の実施
臨床試験に参加される患者さんの人権や安全の確保を図るために、医薬品医療機器等法やGCP※を遵守して治験実施計画書を作成するとともに、インフォームド・コンセントを患者さんからいただいています。
また、「社内治験審査委員会」を設置し、社外の医学専門委員を交えて試験の倫理的および科学的な妥当性を評価しています。
海外での臨床試験においてもICH※-GCPを遵守するとともに、各国の規制要件やガイドラインに従って実施しています。
※GCP(医薬品の臨床試験の実施の基準):医薬品の臨床試験を適切に実施するための基準
※ICH(医薬品規制調和国際会議):医薬品の承認審査基準に関する調和を図るためのガイドラインを作成する国際会議
商品の信頼性保証の取り組み
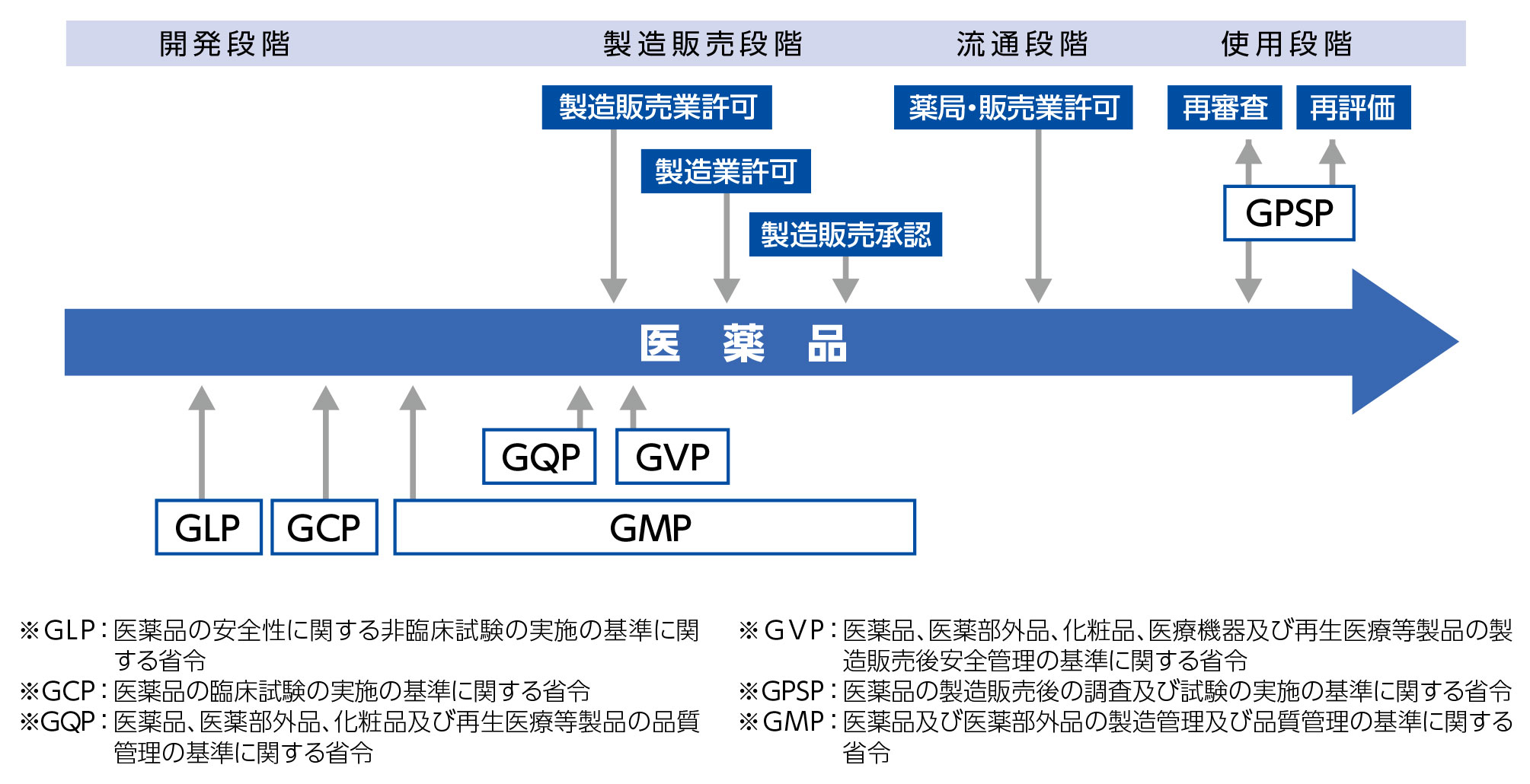
医薬品は、生命に関わる製品であることから、その信頼性を確保するために研究・開発、製造、販売、使用の各段階で数多くの管理基準の遵守が義務付けられています。研究・開発段階ではGLPやGCP、製造段階ではGMP、販売された後はGQPやGVPなど厳しい管理基準が設けられています。
当社では、当社の商品が、これらの管理規準を遵守していることを監査により保証するための専門部門として、信頼性保証部を設置しています。
近年の医薬品の研究・開発、製造、販売、使用のグローバル化に伴い、国際的な調和された管理基準に則り、国内外で適切に監査を行うことにより、当社商品の信頼性を確保しています。
VOICE
『信頼』とは
「信頼」は、その人の実績や過去の振る舞いを見た上で、人間性や人格まで含めて信じてもらえることです。「信頼」は気持ちと気持ちのつながりですから、双方向です。私が所属する信頼性保証部は、まさに信頼性を極める部門です。
私は業務の上で五感を研ぎ澄ませ利用することを大切にしており、特に、「観・感・勘」を使うことを意識しています。まず観察する観、次にそこから何か感じ取ることの感、最後に何かおかしいと働く勘、この3つのカンを磨いています。
これらの五感を上手に活用することで、信頼が信頼を生む善循環のきっかけを作り、信頼性を極めることを常日頃から心がけています。

医薬品の開発から販売使用に至るまでの管理基準